Den Schweregrad von COVID-19 besser einschätzen
02.12.2021
Biomediziner finden im Blut von COVID-19-Patienten einen neuen Marker. Er liefert Einblicke in das Krankheitsgeschehen und könnte zu besseren Diagnosen führen.
02.12.2021
Biomediziner finden im Blut von COVID-19-Patienten einen neuen Marker. Er liefert Einblicke in das Krankheitsgeschehen und könnte zu besseren Diagnosen führen.
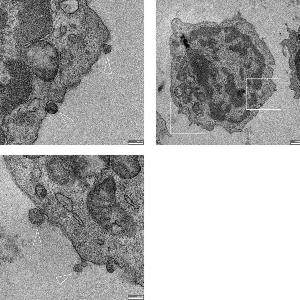
An der Zelloberfläche haften extrazelluläre Vesikel (Pfeile). Bild: M. Schifferer, DZNE
Infektionen mit SARS-CoV-2 laufen bei vielen Patienten symptomlos ab oder verursachen kaum Beschwerden. Sie können aber auch zu dem Krankheitsbild COVID-19 mit Veränderungen der Blutgerinnung und mit Entzündungen führen. Darüber hinaus beobachten Ärztinnen und Ärzte bei COVID-19 Störungen des Immunsystems mit niedrigen Lymphozyten-Titern im Blut.
„Wir wussten bisher, dass ein Zusammenhang zwischen Komponenten der Blutgerinnung und der Immunreaktion besteht“, sagt Prof. Dr. Thomas Brocker, der am Biomedizinischen Centrum der LMU forscht. „Die Gründe und die Mechanismen waren aber weitgehend unbekannt“, so der Wissenschaftler.
Im Fachmagazin Journal of Extracellular Vesicles berichtet Brocker jetzt zusammen mit Kolleginnen und Kollegen über die Rolle von Phosphatidylserin bei COVID-19: einem Molekül, das normalerweise in Zellwänden vorkommt. Es könnte bei pathophysiologischen Mechanismen rund um das Immunsystem und die Blutgerinnung bedeutsam sein, eignet sich perspektivisch aber auch als neuer Biomarker, um per Bluttest die Schwere der Erkrankung zu prognostizieren.
Brockers Labor hatte bereits früher einen Test entwickelt, der Phosphatidylserin in oder auf Blutzellen erkennt. Im Rahmen der Studie untersuchten die Forschenden zwischen April 2020 und Februar 2021 Blutproben von 54 Patienten aus dem COVID-19-Register der LMU (CORKUM). Alle Erkrankten hatten COVID-19 in unterschiedlichen Schweregraden. Hinzu kamen Proben von 35 gesunden und 12 genesenen Spendern. Das Augenmerk der Studie lag auf mononukleären Zellen des peripheren Blutes wie Lymphozyten und Monozyten.
Alle Immunzellen wurden mit dem Phosphatidylserin-Test analysiert und per Durchflusszytometrie, einem physikalischen Verfahren, aufgetrennt. Das Gerät fertigte gleichzeitig mikroskopische Aufnahmen jeder Zelle an. Anhand der Bilddateien konnten die Forschenden erkennen, ob – beziehungsweise wo – sich Phosphatidylserin befand. Dabei zeigte sich, dass die Immunzellen das Signal nicht im Inneren trugen. „Lymphozyten aus dem Blut von COVID-19-Patienten waren mit Bruchstücken von Blutplättchen oberflächlich beladen, was wir anhand des Signals nachweisen konnten“, sagt Brocker. Blutplättchen wiederum beschleunigen die Blutgerinnung. „Damit könnte Phosphatidylserin als Signalgeber für fehlgeleitete entzündliche Prozesse oder Störungen der Blutgerinnung bei COVID-19 dienen, sprich typische Veränderungen bei COVID-19 triggern“, vermutet der LMU-Wissenschaftler.
Bei den Messungen zeigte sich auch eine Assoziation zwischen dem Schweregrad von COVID-19 und Phosphatidylserin. Erhöhte Werte während der aktiven Phase von COVID-19 korrelierten stark mit dem Schweregrad der Erkrankung und könnten perspektivisch zu besseren Diagnosen führen. „Als Marker übertraf Phosphatidylserin etablierte Labormarker für Entzündungsvorgänge im Körper, für Leukozyten und für Gerinnungsfaktoren, die momentan zur klinischen Bewertung von COVID-19 herangezogen werden“, so Brocker. Zur Einstufung werden momentan diverse Laborparameter herangezogen. Sie sind Grundlage der WHO-Skala von null Punkten (gesund) bis hin zu acht Punkten (Tod durch COVID-19).
Noch ist Brockers System für Forschungslabore ausgelegt; die wenigsten Kliniken haben Durchflusszytometer mit Möglichkeiten der Bildgebung. Deshalb wollen die LMU-Forscher jetzt herausfinden, ob sich normale Durchflusszytometer, wie sie viele Krankenhäuser im Labor haben, ebenfalls zur Messung eignen.
Lisa Rausch, Konstantin Lutz, Martina Schifferer, Elena Winheim, Rudi Gruber, Elina F. Oesterhaus, Linus Rinke, Johannes C. Hellmuth, Clemens Scherer, Maximilian Muenchhoff, Christopher Mandel, Michael Bergwelt-Baildon, Mikael Simons, Tobias Straub, Anne B. Krug, Jan Kranich, Thomas Brocker: Binding of phosphatidylserine-positive microparticles by PBMCs classifies disease severity in COVID-19 patients. Journal of Extracellular Vesicles 2021